Наука и нейроны: технологии, возвращающие контроль над телом и памятью
Болезнь Альцгеймера и болезнь Паркинсона ежегодно поражают миллионы людей, ухудшая качество их жизни и ложась тяжелым бременем на семьи больных и систему здравоохранения. Но сегодня мы становимся свидетелями серьезного сдвига: российские ученые предлагают решения, которые соединяют достижения молекулярной биологии, цифровых технологий и клинической неврологии. Эти разработки не просто обещают — они уже реализуются на практике, предлагая пациентам реальную помощь.
Клеточная защита мозга: новое слово в терапии Альцгеймера
Одно из самых многообещающих направлений — борьба с болезнью Альцгеймера. Это тяжелое нейродегенеративное заболевание, которое разрушает память и когнитивные функции человека. В мозге таких пациентов скапливаются токсичные белки — амилоиды и тау-белки, что приводит к гибели нейронов и нарушению связей между ними.
Но сегодня в России появился по-настоящему инновационный подход, способный изменить представления о лечении этого заболевания. Ученые из Российского университета дружбы народов (РУДН) разрабатывают лекарство для защиты мозга от разрушения, вызванного болезнью Альцгеймера. Основу будущего препарата составляют особые молекулярные «посылки» — так называемые везикулы. Это микроскопические пузырьки, которые клетки используют для передачи информации друг другу. Внутри них — белки, РНК и другие вещества, управляющие работой клеток.
Получают везикулы из глиальных клеток — специальных клеток в мозге, которые поддерживают, питают и защищают нейроны (прим. ред.: основные нервные клетки, отвечающие за память, мышление и движение).
В отличие от некоторых существующих препаратов, которые создают из тканей животных, новая разработка создается на основе человеческих клеток и не содержит чужеродных компонентов, тем самым снижается риск побочных реакций, лечение становится более безопасным.
Препарат уже прошел испытания на мышах с моделью болезни Альцгеймера. Результаты оказались впечатляющими:
- снижение количества амилоидных бляшек — вредных белковых отложений в мозге, которые мешают работе нейронов и считаются одним из главных признаков болезни;
- улучшение памяти и способности к обучению — у подопытных животных восстановились когнитивные функции;
- безопасность — не было зафиксировано ни одного серьезного побочного эффекта.
Механизм действия этого препарата основан на том, что везикулы активируют работу гиппокампа — области мозга, которая отвечает за запоминание и обучение. Кроме того, они могут запускать процессы восстановления нервных связей и усиливать естественные механизмы защиты мозга.

Очень важно, что этот разработанный препарат не просто снимает симптомы, а может влиять на саму причину заболевания. То есть он способен замедлять или даже останавливать разрушение мозга, а не только маскировать его последствия.
Пока исследование находится на этапе доклинических испытаний: проводятся тесты на животных. Следующий шаг — тестирование на добровольцах. Если и на этом этапе препарат покажет эффективность и безопасность, он может стать первым в России лекарством, реально защищающим мозг от болезни Альцгеймера.
Успеть вовремя: как распознать Паркинсона до первых симптомов
Болезнь Альцгеймера — не единственное нейродегенеративное заболевание, для которого критически важна ранняя диагностика и своевременное медицинское вмешательство. Не менее остро эта задача стоит и в случае болезни Паркинсона — еще одного серьезного неврологического нарушения, поражающего мозг.
Болезнь Паркинсона обычно диагностируют тогда, когда ее проявления становятся уже заметны — дрожание рук, замедленные движения, нарушение координации. Как правило, к этому моменту в мозге уже утрачено до 70% нейронов, отвечающих за выработку дофамина — вещества, необходимого для нормальной работы двигательной системы. Поэтому одна из важнейших задач современной науки — научиться распознавать болезнь до того, как она проявится клинически, то есть задолго до видимых симптомов.
Именно этим занимаются специалисты Института высшей нервной деятельности и нейрофизиологии РАН (ИВНД РАН). Их исследования направлены на поиск так называемых нейрофизиологических маркеров — объективных показателей, по которым можно судить о начале и скорости развития болезни. В центре внимания — изменения в работе мозга, которые можно зафиксировать с помощью электроэнцефалографии (ЭЭГ) и транскраниальной магнитной стимуляции (ТМС).
ЭЭГ — это метод, который регистрирует электрическую активность мозга. Он позволяет увидеть, как нейроны взаимодействуют между собой, как изменяется ритм их работы при разных задачах. ТМС, в свою очередь, используется для того, чтобы оценить реакцию мозга на внешние сигналы и выявить скрытые нарушения в его функциональных связях.

В рамках проекта ученые анализируют, как изменяются эти показатели у людей с разной степенью риска развития болезни Паркинсона. Это может быть, например, снижение активности в моторных зонах мозга еще до появления дрожания рук или других симптомов. Такие изменения и есть потенциальные биомаркеры — биологические признаки, по которым можно предсказать заболевание на самых ранних этапах.
Создание надежной системы ранней диагностики даст врачам не просто шанс начать лечение раньше — оно откроет возможность персонализированного подхода к каждому пациенту, основанного на индивидуальных нейрофизиологических характеристиках. А значит, появится шанс замедлить или даже предотвратить развитие болезни.
Таким образом, исследования ИВНД РАН — это не только вклад в фундаментальную науку, но и важный шаг к тому, чтобы в будущем болезнь Паркинсона перестала быть приговором, а стала контролируемым состоянием, обнаруживаемым до первых симптомов.
Другая группа исследователей из Пироговского университета во главе с профессором Вадимом Негребецким сделала неожиданное открытие. Во время обычного эксперимента они получили совершенно новые химические вещества, которых раньше не существовало. С помощью специальных методов: рентгеноструктурного анализа и спектроскопии ядерного магнитного резонанса ученые подтвердили уникальную структуру веществ. В ходе различных тестирований на лабораторных мышах с болезнью Паркинсона некоторые из этих веществ улучшали их состояние. Это означает, что на их основе можно создать новые лекарства. Пока до этого еще далеко: сейчас ученые сосредоточены на изучении точных молекулярных механизмов действия веществ и их безопасности. Если исследования пройдут успешно, через несколько лет могут появиться новые, более эффективные лекарства от болезни Паркинсона.
Нейроанализ в кармане: как мобильные технологии меняют возможности диагностики
Тремор — это непроизвольное дрожание рук, часто возникающее у пациентов с болезнью Паркинсона — и служит важным индикатором тяжести заболевания. До недавнего времени оценивать тремор можно было только при очном визите к врачу, и чаще всего — субъективно. Однако сегодня в распоряжении пациентов появляется новый инструмент: мобильное приложение CYPD (Control Your Parkinson`s Disease), разработанное специалистами компании «Ай-Форс».
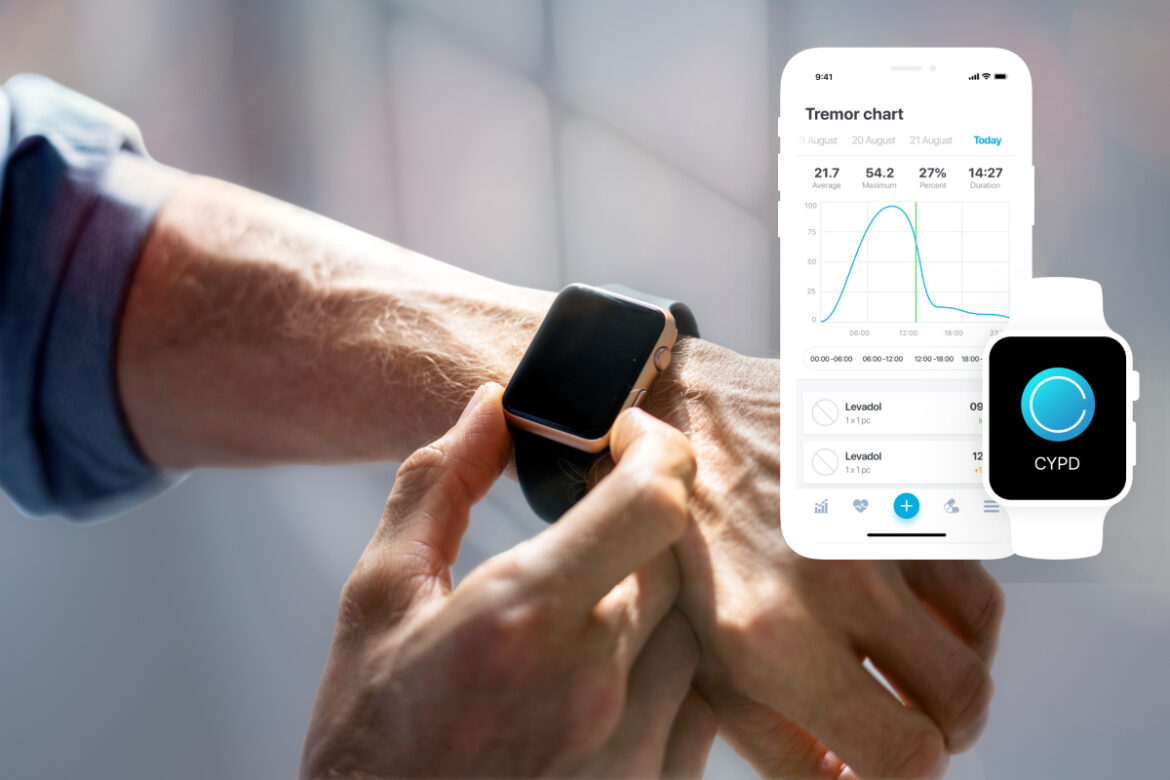
Оно позволяет объективно и в реальном времени отслеживать проявления тремора в домашних условиях с помощью обычных смарт часов. Устройство регистрирует мельчайшие подвижности кисти с помощью гироскопа, а алгоритмы машинного обучения анализируют данные и строят подробные графики колебаний. Пациент может самостоятельно наблюдать динамику своего состояния, а врач получает возможность оценить эффективность терапии не на глаз, а по цифрам.
Пилотные испытания прошли в неврологическом отделении Федерального центра мозга и нейротехнологий ФМБА России, а сама платформа уже используется пациентами в России, Европе и США.
«Результаты мониторинга в виде графиков используются для убеждения пациентов в положительном влиянии лекарственных препаратов, что способствует их приверженности лечению» — Дмитрий Катунин, врач-невролог «Федерального центра мозга и нейротехнологий» ФМБА России.
CYPD — пример того, как цифровая медицина становится частью регулярного мониторинга состояния при болезни Паркинсона и других двигательных расстройствах.
Новая глава в российской неврологии
Сегодня отечественная наука уверенно выходит за пределы лаборатории и вступает в эпоху трансляционной медицины – подхода, при котором результаты фундаментальных исследований находят реальное применение и все чаще переходят в клиническую практику врача, а не остаются лишь на бумаге. Трансляционную медицину можно определить как «междисциплинарную область, опирающуюся на три основных направления: лабораторный, клинический и общественный». Ее цель состоит в том, чтобы объединить дисциплины, ресурсы, опыт и методы в рамках этих направлений для улучшения профилактики, диагностики и лечения. Например, вещество, изученное в лаборатории, со временем может лечь в основу нового препарата, а экспериментальная методика — стать цифровым приложением, позволяющим пациенту контролировать свое состояние дома.

Российские ученые активно развивают это направление: создают молекулы, защищающие клетки мозга, разрабатывают мобильные технологии для отслеживания тремора и ищут ранние биомаркеры, способные выявить болезнь задолго до появления первых симптомов.
Главный акцент сегодняшняя медицинская наука делает не на лечении последствий, а на раннем вмешательстве, профилактике и персонализированном подходе. Это означает, что вместо стандартных схем терапии появляются гибкие решения, адаптированные к конкретному человеку с учетом его нейрофизиологии, биомаркеров, образа жизни и цифровых данных.
Такой подход не только дает больше шансов на эффективность лечения, но и меняет саму философию медицины. Болезни, которые еще недавно воспринимались как приговор, в том числе и нейродегенеративные заболевания, такие как болезнь Альцгеймера и Паркинсона, при таком подходе могут стать управляемыми процессами. И хотя до полного излечения пока далеко, возможности науки уже позволяют влиять на течение заболевания, отодвигать его начало, снижать интенсивность симптомов и поддерживать качество жизни пациентов на высоком уровне.
Будущее уже приходит — не как революция, а как ежедневная работа врачей, исследователей, инженеров и программистов, которые вместе строят новую медицину: точную, цифровую, превентивную. И в этой новой системе роль пациента тоже меняется — он становится активным участником своего лечения, а не пассивным объектом наблюдения. Именно так формируется наука о мозге завтрашнего дня — наука, которая возвращает человеку контроль над собственными мыслями, эмоциями и поведением, позволяя лучше понимать себя и управлять своей жизнью.
Анастасия Будаева
Изображение на обложке: Freepik
Создано при поддержке Минобрнауки РФ в рамках Десятилетия науки и технологий (ДНТ), объявленного Указом Президента Российской Федерации от 25 апреля 2022 г. № 231.